Introduzione
Il fisiologico riassorbimento del processo alveolare in senso cranio-caudale e vestibolo-palatale in seguito alla perdita degli elementi dentari spesso non permette il posizionamento di impianti osteointegrati nella zona posteriore del mascellare superiore senza un’adeguata ricostruzione ossea.
I carichi funzionali esercitati sulla cresta residua che si trasformano in carichi compressivi, favoriscono il riassorbimento osseo in senso centripeto e cranio-caudale (Cawood et al. 1988) con conseguente riduzione dimensionale del processo alveolare associata da una progressiva pneumatizzazione del seno mascellare.
Tra le procedure chirurgiche preimplantari proposte per ripristinare il volume osseo perso, la chirurgia del seno mascellare ha dimostrato di essere una procedura con elevata predicibilità clinica (Wallace et al. 2003, Del Fabbro et al. 2004-2008-2012-2013 a-b, Pjetursson et al. 2008, Testori et al. 2012). L’approccio laterale è utilizzato in presenza di atrofia ossea con osso residuo inferiore a 4/mm senza deficit ossei nei tre piani dello spazio che compromettono la costruzione di una protesi corretta.
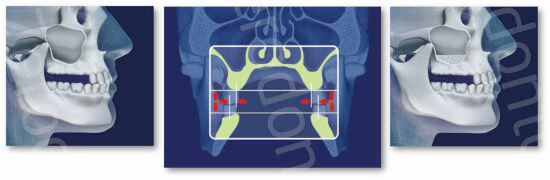
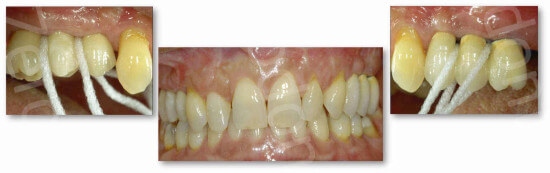
Se sono presenti altri deficit ossei orizzontali e/o laterali è indicato ricostruire la cresta ossea in modo tridimensionale.
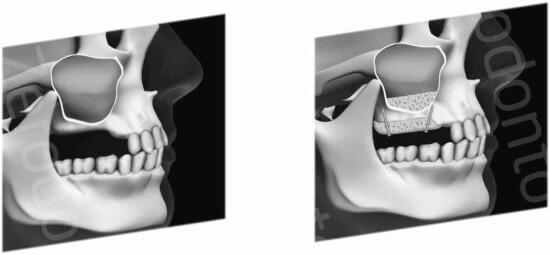
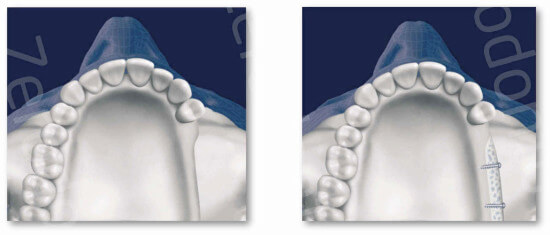
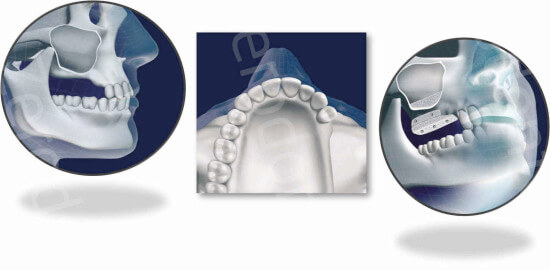
In caso di atrofie di minore entità con altezza della cresta ossea residua superiore ai 4 mm, si può procedere con una tecnica meno invasiva che comporta un approccio crestale descritto per la prima volta da Summer (osteotome technique) (Summers 1994) e successivamente rivisto da numerosi autori. (Del Fabbro et al. 2012)
Nella fase di pianificazione chirurgica occorre considerare, oltre alla conoscenza dell’anatomia e della fisiologia del seno mascellare, eventuali patologie naso-sinusali, che devono essere diagnosticate pre-operatoriamente e in alcuni casi valutate in collaborazione con uno specialista otorinolaringoiatra. Al fine di identificare, in una fase preventivo-diagnostica, tutte quelle condizioni che, dal punto di vista ORL costituiscono una controindicazione assoluta o relativa all’elevazione del seno mascellare (Mantovani M et al. 2005) sono utili specifiche indagini radiologiche tridimensionali quali una TC o una CBCT, che allo stato attuale delle conoscenze è più indicata per la riduzione della dose assorbita dal paziente. (Ludlow et al. 2008)
Protocolli chirurgici – Approccio laterale
1) Corretta procedura anestesiologica
Una corretta tecnica anestesiologica è un prerequisito fondamentale per un’efficace procedura chirurgica e prevede un’infiltrazione lenta, (velocità di 1 ml/min), profonda, che non deve distendere i tessuti alterando la morfologia del fornice, al fine di ottenere una maggior efficacia e durata dell’effetto anestetico. Il farmaco di prima scelta è l’articaina cloridrato 4% con adrenalina 1.100.000 che ha un tempo di latenza di circa 2 minuti (Costa et al. 2005). Il razionale nell’esecuzione dell’anestesia prevede l’infiltrazione partendo a livello disto-vestibolare, proseguendo a livello mesio-vestibolare, successivamente disto-palatale e mesio-palatale. Normalmente 2 tubofiale da 1.8 cc iniettate in un tempo di 2 minuti per tubofiala sono sufficienti per ottenere l’effetto desiderato. L’infiltrazione eseguita anche a livello dell’angolo della bocca, permette di poter posizionare i retrattori senza creare discomfort al paziente. L’esecuzione di anestesie locali superficiali, eseguite in modo troppo rapido, distendendo i tessuti determinano un effetto analgesico meno duraturo nel tempo.
2) Disegno del lembo
Prima di eseguire il lembo di accesso è opportuno tenere in considerazione i seguenti punti:
- posizione mesio-distale del seno
- posizione ideale dell’antrostomia
- quantità di gengiva aderente sul versante vestibolare
- presenza/assenza di denti
L’estensione dell’incisione deve anticipare eventuali manovre di rigenerazione ossea che il chirurgo potrà mettere in atto durante l’intervento e come concetto generale deve essere più ampio della proiezione del seno mascellare nella parete ossea vestibolare della maxilla. È opportuno ricordare che mediante l’elevazione del seno mascellare non vengono alterati i rapporti ossei intermascellari. L’incisione deve essere a tutto spessore può essere crestale o più spostata verso il palato.
Quest’ultima variante è consigliabile nel caso in cui esista una inserzione muscolare a livello crestale o se la gengiva aderente è inferiore a 2/3 mm dal centro della cresta alla giunzione muco-gengivale.
La presenza di almeno 3 mm tessuto cheratinizzato sul lembo vestibolare facilita la sutura.
Se il seno si estende in zona primo premolare/canino, si consiglia una incisione mesiale al canino a mazza da hockey, bisellata a spessore totale in gengiva aderente a partenza dal punto di passaggio tra il lato vestibolare e approssimale (line-angle) dell’elemento dentale
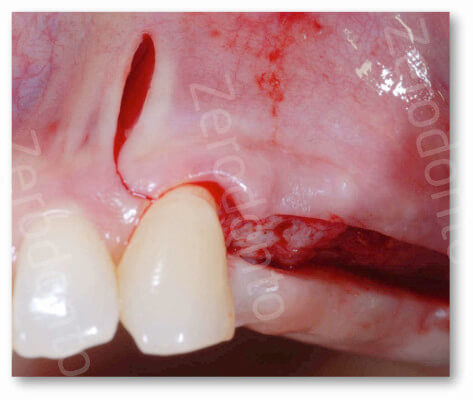
e a spessore parziale in mucosa alveolare per evitare lesioni neurologiche al nervo infraorbitario.

Se il seno è situato in zona 1°/2° premolare, l’incisione inizierà distale al canino.
A seconda della situazione clinica, l’incisione potrà essere intrasulculare o paramarginale.
La prima è consigliata in presenza di denti naturali esenti da malattia parodontale e si conclude con una tecnica micro-chirurgica di sutura. Se i denti sono pilastri di protesi, si preferisce una incisione paramarginale apicale alla profondità di sondaggio soprattutto in caso di biotipi parodontali sottili.
Se è contemplato un prelievo osseo dal tuber, l’incisione crestale potrà estendersi fino ad esso per permettere l’esposizione contemporanea della sede donatrice.
L’incisione di rilascio verticale deve estendersi parallelamente all’apporto vascolare e dipenderà dall’estensione del seno stesso e dalla posizione prevista per l’antrostomia.
3) Scollamento
Il lembo è a spessore totale e dunque lo scollatore deve agire aderente al piano osseo durante le fasi di scollamento in modo che il periostio non venga danneggiato.
Un corretto disegno e scollamento del lembo, lasciando integro il periostio, permettono di avere un ottimale controllo dell’emostasi, che tuttavia dipende anche da altri fattori quali la condizione medica del paziente, i farmaci assunti e la tecnica anestesiologica utilizzata.
Una volta evidenziato il piano osseo si potranno distinguere una porzione corticale che si presenterà esente da sanguinamento, mentre le zone con midollare sottostante sanguineranno. In alcuni casi si potrà notare il decorso dell’anastomosi dell’arteria alveolare postero-superiore con l’arteria infraorbitaria.
Qualora fosse presente un eccessivo sanguinamento è suggerita la compressione con garze umide per 5 minuti a livello del fornice vestibolare prima di procedere con l’esecuzione dell’antrostomia.
Questa manovra ridurrà il sanguinamento. In casi in cui si evidenzia a livello della CBCT/TC pre-operatoria una mancanza di corticale ossea vestibolare il chirurgo dovrà procedere con attenzione durante lo scollamento dissezionando con cura il lembo mucoso della membrana sinusale.
4) Antrostomia
Il posizionamento dell’antrostomia è determinato dall’estensione del seno mascellare.
L’antrostomia può essere agevolmente eseguita, sotto abbondante irrigazione di soluzione fisiologica refrigerata, mediante un manipolo dritto ad alta velocità (40.000 giri/minuto) e fresa al carburo di tungsteno di diametro ISO 1.8; quando in prossimità della membrana del seno il colore della membrana stessa comincia a trasparire, virando verso il blu, è suggerito utilizzare una fresa diamantata di grana media ISO 1.8 che risulta meno traumatica in caso di accidentale contatto con la sottile membrana sinusale. Nei casi in cui si presenta una corticale sottile e si nota trasparire il colore blu della membrana appena scollato il lembo, si suggerisce di eseguire l’antrostomia con la fresa diamantata.
Per eseguire l’antrostomia è possibile utilizzare una tecnica piezoelettrica che riduce la possibilità di perforazioni accidentali (Vercellotti et al. 2001).
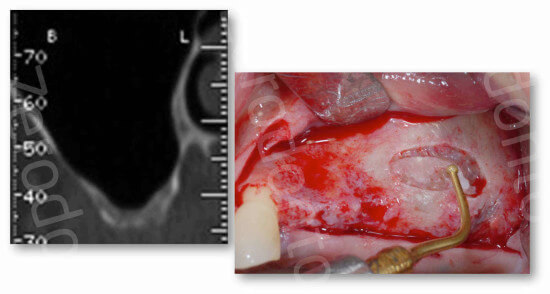
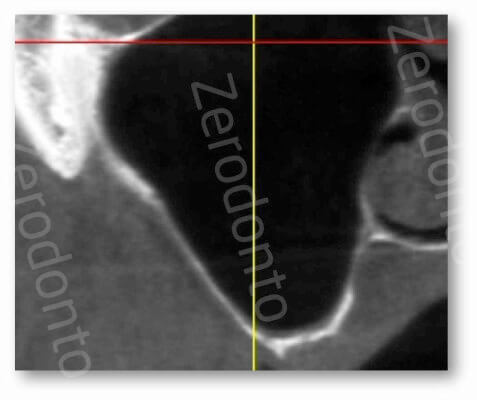
Se lo spessore della parete ossea è maggiore di 1 mm, la corticale può essere ridotta con un inserto di osteoplastica
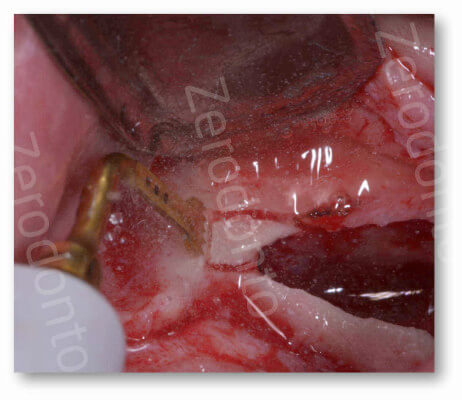
utilizzato per eseguire ostectomie o utilizzare un inserto piezoelettrico raccogliendo tessuto osseo che verrà utilizzato come materiale da innesto.
L’antrostomia solitamente ha una forma ovale senza margini acuti che possono causare sanguinamenti della membrana Schneideriana durante le fasi operative successive.
La dimensione dell’antrostomia dipende dal numero di impianti che dovranno essere inseriti, mediamente una dimensione di 20 mm in senso mesio-distale e 15 mm in senso apico-coronale è sufficiente a garantire un agevole accesso chirurgico. È consigliabile ridurre le dimensioni dell’antrostomia quando la curva di apprendimento dell’operatore è ad un livello tale da consentire una corretta operatività anche con un accesso ridotto (10 mm in senso mesio-distale, 6 mm in senso apico-coronale).
Il margine distale dell’antrostomia è posizionato in relazione al numero di impianti da inserire.
Il margine caudale dell’antrostomia deve trovarsi a 3-4 mm craniale alla base del seno.
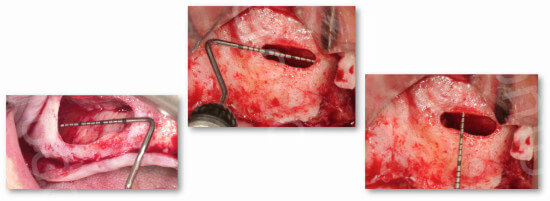
La presenza di setti mascellari (setti di Underwood) può indurre a dover variare la dimensione e posizione dell’antrostomia o, in alcuni casi, obbligare a disegnare due accessi autonomi.
In rari casi è possibile rimuovere interamente il setto, recidendolo alla base.
Un accesso più conservativo permette di risparmiare tessuto osseo che faciliterà la guarigione dell’innesto che avviene in senso centripeto dalle pareti verso il centro dell’innesto.
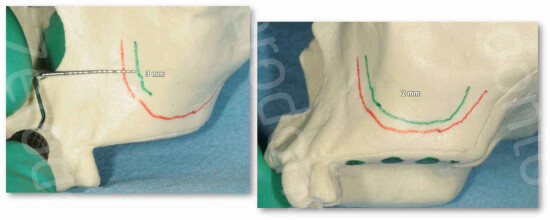
La tecnica può essere modificata in relazione alla posizione e al decorso dell’anastomosi vascolare, per semplificare l’operatività è eseguire l’antrostomia partendo più coronalmente al vaso, in modo da non lederlo (Testori et al 2013)
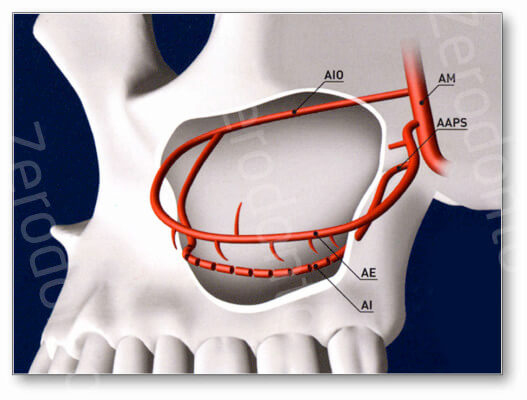
Se il decorso è intraosseo, condizione rilevabile preoperatoriamente mediante CBCT/TC, e il vaso interferisce con l’esecuzione dell’antrostomia, è suggerito recidere il vaso.
Per evitare sanguinamenti intraoperatori o postoperatori è essenziale, qualora venisse recisa l’arteria durante l’operatività, elettro cauterizzare con apparecchi appositi bipolari o utilizzare la cera da osso (Bone Wax Johnson & Johnson Bruxelles, Belgium) sui due tronchi vascolari recisi o legare il vaso in caso di vasi con diametro > 2 mm. (Testori et al 2013)
Il diametro di questo vaso può essere sondato con la sonda parodontale il cui diametro è variabile da 0.5 a 1 mm.
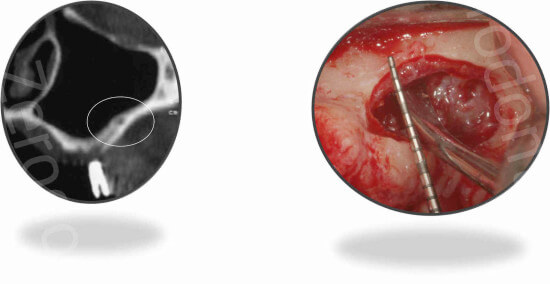

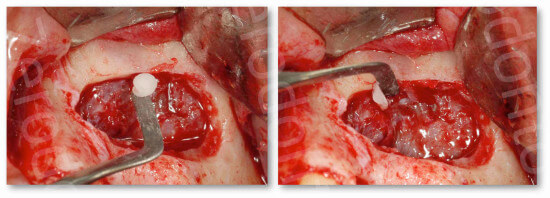

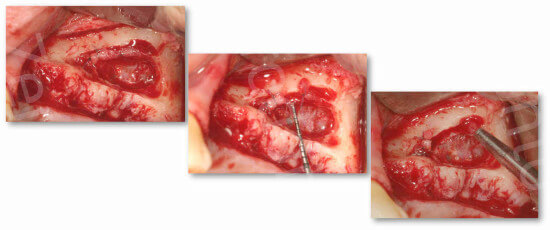
Se il decorso è extraosseo, condizione rilevabile clinicamente, il vaso può mantenersi adeso alla membrana sinusale e quindi viene sollevato con essa.
Terminato l’effetto vasocostrittore dell’anestesia locale, una anastomosi recisa, ma non trattata, può esitare in emorragie a sutura completata o dopo la dimissione del paziente.
Una volta completata l’ostectomia periferica, si testa la mobilità dell’antrostomia e ogni ponte osseo residuo deve essere rimosso prima di tentare di elevare la membrana sinusale. Se si lascia la parte centrale di osso, che viene ribattuta all’interno della cavità subsinusale, attaccata alla membrana sinusale, l’antrostomia viene definita antrostomia per riflessione.
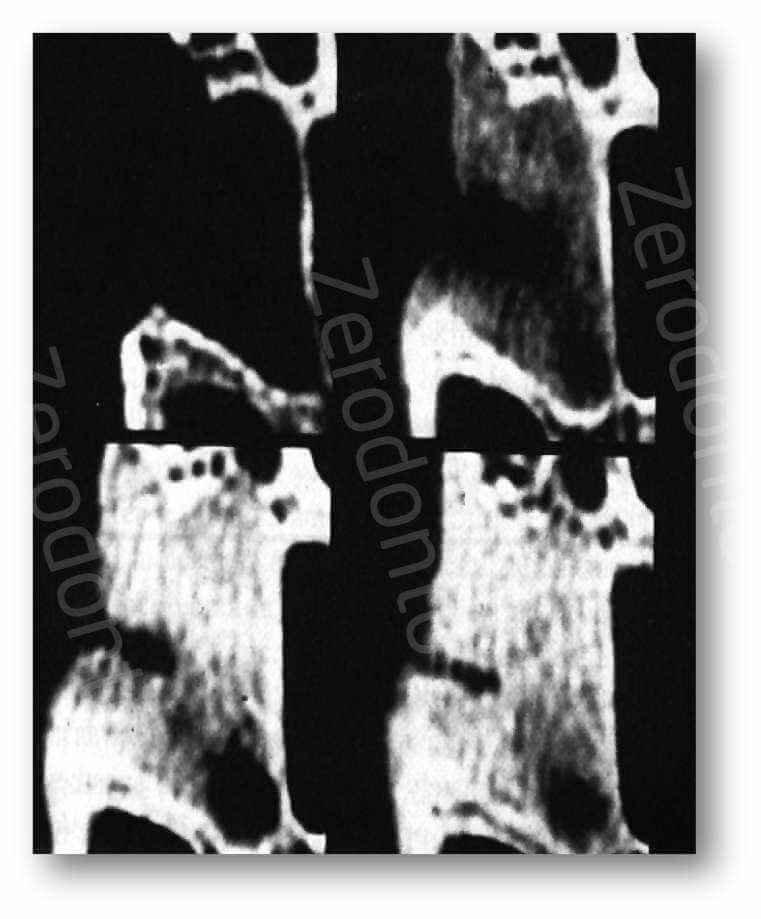
Questo tipo di antrostomia viene utilizzata in caso di pareti ossee il cui spessore è inferiore ad 1 mm. E’ consigliato, invece, erodere l’osso (antrostomia per erosione) nei casi in cui lo spessore della teca fosse > 1 mm (Smiler 1997). Cercare di riflettere una parete ossea più spessa di 1 mm aderente ad una membrana sinusale che in salute è intorno ai 100/500 micron, può esitare più facilmente in perforazione della membrana stessa. (Dia 21-22)

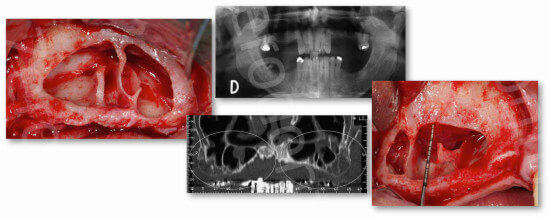
5) Elevazione della membrana sinusale
Una volta completata l’antrostomia, si utilizza un inserto piezoelettrico dedicato che trova un primo piano di clivaggio fra il piano osseo e lato periostale della membrana sinusale lungo i margini dell’antrostomia (Dia 23).
Si prosegue lo scollamento con strumenti chirurgici manuali, che sono più ergonomici e maneggevoli rispetto al manipolo piezoelettrico. Gli strumenti devono esser mantenuti sempre a contatto con il piano osseo esercitando una forza continua e costante per elevare la membrana senza lacerarla.
Lo scollamento della membrana sinusale deve procedere dove presenta minore resistenza, iniziando in corrispondenza del margine superiore dell’antrostomia, proseguendo poi distalmente, mesialmente e infine coronalmente. In caso di resistenza allo scollamento è opportuno mantenersi sempre aderenti al piano osseo sottostante e recidere l’aderenza mediante l’utilizzo di strumenti taglienti (Dia 24-26)
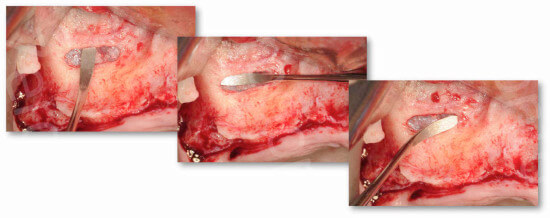


Strumenti smussi in presenza di membrane molto aderenti al piano osseo determinano più facilmente lacerazioni.
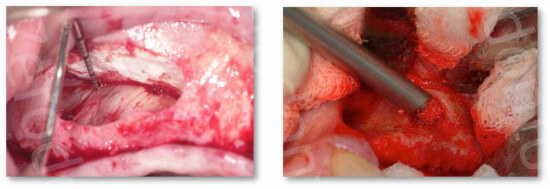
La mucosa deve essere scollata fino ad evidenziare la parete mediale (ovvero la parete laterale del naso) della cavità sinusale. Eseguire solo la lateralizzazione del seno mascellare senza interessare nello scollamento la parete mediale può portare, in seguito alla ripneumatizzazione del seno, una mobilizzazione del materiale da innesto. Scollare fino alla parete mediale permette inoltre di esporre una maggiore superficie ossea che favorisce una migliore guarigione dell’innesto (Margolin et al. 1998) e un posizionamento implantare più favorevole alla riabilitazione protesica (Dia 27).
L’elevazione deve essere eseguita con gli strumenti dedicati e non con il materiale da innesto che deve essere posizionato in modo passivo nel volume ricreato senza esercitare un ulteriore scollamento della membrana. La creazione di un volume predeterminato e passivo è un requisito fondamentale della tecnica chirurgica e previene accidentali perforazioni da parte del materiale che potrebbero rimanere misconosciute e causare dispersione del materiale da innesto nella cavità sinusale (Dia 28-29).
6) Preparazione del sito implantare
Dopo aver elevato la membrana nel seno, se la cresta ossea è di altezza intorno a 3/4 mm, è possibile posizionare simultaneamente gli impianti.
In casi clinici con ossi di tipo 3 e 4 a livello della cresta ossea residua è consigliato sottodimensionare il sito implantare.
Durante l’utilizzo delle frese, il chirurgo dovrà proteggere la membrana del seno per non lederla con gli strumenti rotanti mediante uno scollaperiostio.
Qualora lo spessore osseo fosse inferiore a 3/4 mm è consigliato elevare il seno e posizionare gli impianti ad innesto consolidato, è stato dimostrato come non vi siano differenze statisticamente significative in impianti posizionati simultaneamente all’elevazione o ad innesto consolidato (Del Fabbro et al. 2004).
7) Inserimento del materiale da innesto e posizionamento implantare in caso di approccio simultaneo
Anche in assenza di perforazioni, è consigliabile inserire una membrana riassorbibile non cross-linked per evitare, durante la compattazione dell’innesto, che alcune particelle di biomateriale, soprattutto se si utilizzano innesti con granulometria 1-2 mm di diametro, possano creare delle microperforazioni. Allo stato attuale delle conoscenze non sappiamo se queste microperforazioni abbiano rilevanza dal punto di vista clinico, tuttavia ci sembra ragionevole ipotizzare che sia consigliato preservare l’integrità anatomo–funzionale della membrana sinusale. Un recente studio istologico su umano ha dimostrato che la percentuale di osso vitale è maggiore quando si utilizza osso bovino deproteinizzato con granulometria grande (1-2 mm) rispetto alla granulometria piccola (0.5-1 mm) (Testori et al. 2013). Il materiale da innesto, sia nell’approccio simultaneo che dilazionato, deve essere inserito partendo dalle zone meno accessibili, quindi, nei recessi anteriore e posteriore e successivamente nella zona lungo la parete mediale del seno, posizionando l’innesto a contatto con le pareti ossee per facilitarne i processi di guarigione.
Nel caso in cui si sia pianificato il posizionamento simultaneo degli impianti, dopo aver posizionato circa 2/3 dell’innesto, si inseriscono gli impianti e, successivamente, si completa l’inserimento del biomateriale. Durante questa procedura bisogna controllare in modo efficace l’asepsi del campo chirurgico mediante garze sterili e carrier dedicati (Dia 30-31).
Nei pazienti con biotipo parodontale sottile o in portatori di una protesi rimovibile ad appoggio mucoso, è consigliabile inserire gli impianti in posizione sottocrestale.
Una compattazione eccessiva del materiale da innesto riduce gli spazi tra le particelle del biomateriale impedendone la rivascolarizzazione; questo aspetto risulta particolarmente evidente con l’utilizzo di biomateriali a lento riassorbimento. L’inserimento di impianti a superficie ruvida aumenta in modo statisticamente significativo la percentuale di contatto osso- impianto ed inoltre la percentuale di sopravvivenza è più elevata rispetto alle superfici lisce.
Terminato il riempimento della cavità sinusale, viene posizionata una membrana riassorbibile sulla parete ossea vestibolare, a livello dell’antrostomia. Alcuni studi clinici (Tarnow et al. 2000; Tawill et al. 2001) hanno suggerito che il posizionamento di una membrana riassorbibile sull’antrostomia determini una percentuale di osso vitale superiore ed un successo implantare più elevato rispetto ai siti in cui non veniva posizionata la membrana. Un recente lavoro scientifico (Barone et al. 2013) ha riportato dati in contrasto con i precedenti lavori rilevando che non vi erano differenze statisticamente significative in termini di percentuali di osso vitale rispetto al non utilizzo della membrana. Una recente metanalisi (Torres Garcia-Denche et al. 2013) ha evidenziato come il posizionamento di una membrana a livello dell’anstrostomia non migliori la prognosi della procedura. Un nuovo approccio prevede il posizionamento di una membrana invaginata per 2 mm all’interno dell’antrostomia per prevenire la fuoriuscita del materiale da innesto in caso di accidentale aumento della pressione endosinusale (Testori et al. 2013). L’osso autologo è sempre stato considerato il gold standard dei materiali da innesto per le capacità osteogenetiche, osteoinduttive e osteoconduttive e per questa ragione consigliato durante il periodo di sviluppo della tecnica. Allo stato attuale delle conoscenze non esistono differenze statisticamente significative tra l’utilizzo dei biomateriali e dell’osso autologo in termini di sopravvivenza implantare. (Wallace et al. 2012) Tuttavia quando si valuta l’efficacia dei materiali da innesto è impossibile ignorare che la superficie implantare ruvida giochi un importante ruolo sul risultato clinico finale. La famiglia dei biomateriali che ha più evidenza scientifica è rappresentata dagli xenoinnesti il cui successo può essere attribuito a 3 fattori:
- l’osteoconduttività del biomateriale che determina circa il 25% di osso vitale dopo 6-8 mesi dall’innesto
- il lento riassorbimento aggiunge al futuro sito implantare un ulteriore 25% del contenuto minerale
- i risultati istologici evidenziano che le particelle del biomateriale residuo non sono mai a contatto diretto con la superficie implantare, ma sono circondate ed interconnesse tra loro da osso vitale (bone bridging). (Wallace et al. 2012)
I dati clinici e gli studi istologici uniti alla riduzione dell’invasività della procedura chirurgica, per la mancanza di un sito donatore, sembrano suggerire che i biomateriali rappresentino attualmente il gold standard in questo tipo di chirurgia.
Esistono evidenze istologiche e studi clinici che dimostrano come la maturazione dell’innesto possa essere accelerata miscelando osso autologo al biomateriale, aumentando tuttavia l’invasività dell’intervento (Wallace et al 2012).
Per completezza di esposizione bisogna ricordare che in letteratura sono state riportate alte percentuali di successo con l’utilizzo di materiali alloplastici, anche se le evidenze scientifiche sono meno numerose. (Wallace et al. 2012)
Nell’ultimo decennio abbiamo assistito all’introduzione delle biotecnologie, rappresentate dall’utilizzo delle proteine morfogenetiche imbibiti in una matrice di collagene e dai fattori di crescita ricombinanti. Ad oggi in Italia non sono stati registrati per l’uso clinico ed inoltre il loro utilizzo presenta alcuni aspetti negativi rappresentati da: costi elevati, presenza di osso immaturo nelle fasi precoci di guarigione dell’innesto e riassorbimento dell’innesto stesso. Per diminuire il riassorbimento dell’innesto è stato proposto di aggiungere una certa quantità di particolato di osso omologo (Tarnow et al. 2010) con promettenti risultati clinici, oppure xenoinnesti con un’elevata stabilità dimensionale. In alcuni casi però tali innesti hanno dimostrato risultati istologici peggiori rispetto all’ utilizzo di solo xenoinnesto (Kao et al. 2012). L’utilizzo dei fattori di crescita ricombinanti in associazione ad osso bovino deproteinizzato ha mostrato buoni risultati per quanto riguarda la guarigione dei tessuti molli e un miglioramento della guarigione dell’innesto (Froum et al. 2013). Per quanto riguarda i fattori di crescita omologhi alcuni lavori scientifici hanno evidenziato un effetto positivo anche a livello dei tessuti duri; per contro recenti revisioni sistematiche hanno associato l’effetto positivo soprattutto per quanto riguarda la guarigione dei tessuti molli. Una recente analisi sistematica sull’efficacia dei fattori di crescita nell’elevazione del seno mascellare ha incluso 12 lavori scientifici per un totale di 445 elevazioni del seno mascellare (Del Fabbro et al. 2013). Sei di questi studi, basandosi su analisi istomorfometrica riportano un effetto positivo dei concentrati piastrinici a livello della maturazione ossea. Al contrario altri sei studi non evidenziano una significativa differenza tra il gruppo controllo e il gruppo test che utilizzava i fattori di crescita. Nessuno studio ha evidenziato una differenza nella sopravvivenza implantare. Purtroppo in questi studi è stata riscontrata una ampia eterogeneità riguardante il disegno dello studio, le tecniche chirurgiche applicate, la tipologia di innesto utilizzato ed infine le variabili considerate nelle analisi cliniche ed istomorfometriche. Tutti gli studi inclusi nella revisione sono concordi sull’ effetto positivo dei fattori di crescita sui tessuti molli nelle fasi di guarigione e sul minor discomfort post-operatorio.
In conclusione, allo stato attuale delle conoscenze, non si evidenzia un vantaggio nell’utilizzo dei fattori di crescita nell’elevazione del seno mascellare e sono necessari ulteriori studi clinici randomizzati.
In letteratura esiste (Lundgren et al. 2004, Cricchio et al. 2011) una tecnica alternativa che prevede l’utilizzo, in caso di inserimento implantare simultaneo, del solo coagulo ematico di collagene o di soli fattori di crescita omologhi (Mazor et al. 2009) posti al di sotto della membrana sinusale. Il razionale di tale approccio è che gli impianti creano un effetto tenda sostenendo la membrana e favorendo quindi la neoformazione ossea nelle zone interimplantari.
Nei casi in cui non viene utilizzato un materiale da riempimento non si verifica una rigenerazione ossea; oltre l’apice implantare di solito la rigenerazione è più coronale lasciando, le ultime spire che radiologicamente sembrano protrudere all’interno del seno, a contatto con la membrana sinusale.
L’approccio clinico utilizzato dagli Autori è basato sulle revisioni sistematiche pubblicate in letteratura, in cui si evidenzia che i fattori prognostici favorevoli per raggiungere il successo clinico sono:
- utilizzo di impianti a superfice ruvida
- utilizzo di biomaterali soprattutto xenoinnesti.
- posizionamento di una membrana all’interno dell’antrostomia non tanto per aumentare la percentuale di osso vitale all’interno dell’innesto ma per prevenire la fuoriuscita dello stesso a livello del forame (Dia 32-34)
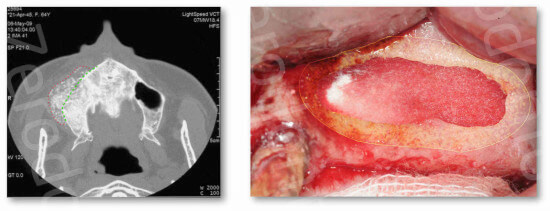
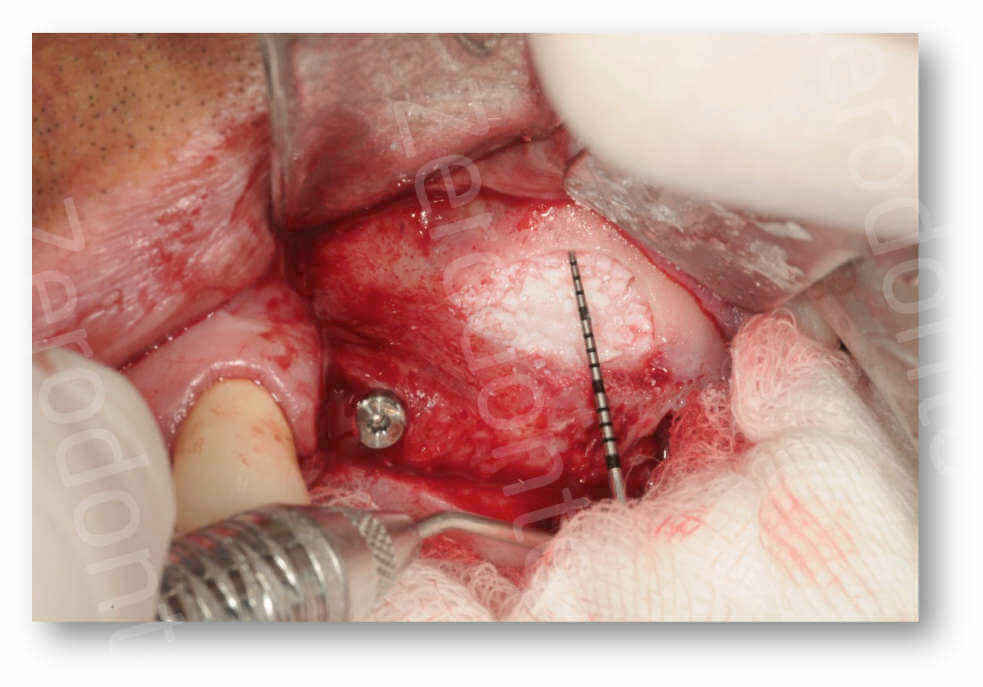
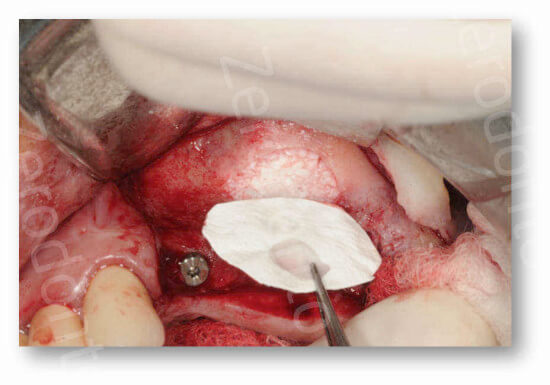

Da ultimo, per quanto riguarda i tempi di attesa, si suggerisce nei casi di elevazione del seno mascellare con l’utilizzo di soli biomateriali di attendere un tempo compreso tra i 6 e i 9 mesi prima di posizionare gli impianti nel caso di approccio dilazionato, o prima di eseguire la seconda fase chirurgica in caso di approccio simultaneo.
8) Sutura
Il lembo deve poter ritornare in cresta in modo passivo, senza trazioni, eventualmente, per passivarlo, si possono eseguire delle incisioni periostali di rilascio.
È consigliabile cominciare la sutura apicalmente a livello dell’incisione di rilascio mesiale.
A livello crestale possono essere utilizzati punti a materassaio orizzontale o suture continue.
Il tipo di sutura da utilizzare dipende dal tipo di tessuto: in gengiva aderente è consigliato un monofilamento non riassorbibile, mentre in caso di mucosa alveolare viene indicata una sutura riassorbibile, in alternativa si può suturare tutto il lembo con suture riassorbibili.
9) Raccomandazioni cliniche per ridurre l’incidenza di complicanze intra e post-operatorie
Pur essendo la procedura predicibile e la percentuale di complicanze molto ridotta, si consiglia di attenersi alle raccomandazioni cliniche durante tutte le procedure operative:
- Raccolta dell’anamnesi e valutazione delle eventuali terapie farmacologiche assunte dal paziente
- Adeguata selezione del caso clinico con seno sano e ventilato
- Risoluzione preventiva delle eventuali patologie endodontiche e parodontali a livello orale
- Adeguata profilassi antibiotica
- Contenimento degli indici di placca (FMPS) e di sanguinamento (FMBS) con valori non superiori al 15%
- Rimuovere le eventuali corone provvisorie e detergere i monconi con soluzione antisettica (derivati iodati o clorexidina) rimuovendo tutto il cemento dal solco gengivale e dal moncone protesico
- Disinfezione della cute con antisettici cutanei (derivati iodati o clorexidina) e sciacqui con clorexidina a livello del cavo orale
- Allestimento di un campo sterile con mantenimento della catena di sterilità
- Mantenimento delle linee di incisione distanti dall’antrostomia e dall’eventuale membrana
- Prevenzione dalla contaminazione dell’innesto e delle membrane
- Controllo intra- e post-operatorio dell’emostasi
- Evitare il surriscaldamento dell’osso
- Mantenimento della sterilità dello strumentario (consigliato un set per l’elevazione del seno diverso dal set chirurgico per l’allestimento del lembo)
- Abbondanti lavaggi del campo operatorio con soluzione fisiologica
- Contenimento dei tempi operatori
- Sciacqui con clorexidina nel periodo post-operatorio
- Adeguata terapia post-operatoria
- Monitoraggio del paziente: settimanalmente durante il primo mese e mensilmente nei successivi tre mesi
Si può concludere dicendo che l’elevazione del seno mascellare è una tecnica ricostruttiva predicibile con una bassa percentuale di complicanze intra e post-operatorie a patto che si segua scrupolosamente la corretta tecnica chirurgica e le sopracitate raccomandazioni cliniche.
BIBLIOGRAFIA
- Cawood JI, Howell RA. A classification of the edentulous jaws. Int J Oral Maxillofac Surg. 1988;17:233-236.
- Wallace SS, Froum SJ. Effect of maxillary augmentation of survival of endosseous dental implants. A systematic review. Ann Periodontol. 2003;8 328-343.
- Del Fabbro M, Testori T, Francetti L, Weinstein RL. Systematic review of survival rates for implants placed in the grafted maxillary sinus. J Periodontics Restorative Dent. 2004;24:565-577.
- Del Fabbro M, Rosano G, Taschieri S. Implant survival rates after maxillary sinus augmentation. Eur J Oral Sci 2008;116:497-506.
- Del Fabbro M, Corbella S, Weinstein T, Ceresoli V, Taschieri S. Implant survival rates after osteotome-mediated maxillary sinus augmentation: a systematic review. Clin Implant Dent Relat Res. 2012;14:s159-168.
- Del Fabbro M, Bortolin M, Taschieri S, Weinstein RL. Effect of autologous growth factors in maxillary sinus augmentation: a systematic review. Clin Implant Dent Relat Res. 2013a;15:205-216.
- Del Fabbro M, Wallace SS, Testori T. Long-term implant survival in the grafted maxillary sinus: a systematic review. Int J Periodontics Rest Dent 2013b;33:773-783.
- Pjetursson BE, Tan WC, Zwahlen M, Lang NP. A systematic review of the success of sinus floor elevation and survival of implants inserted in combination with sinus floor elevation. Part I: lateral approach J Periodontol. 2008;35:216-240.
- Testori T, Weinstein RL, Taschieri S, Del Fabbro M. Risk factor analysis following maxillary sinus augmentation: a retrospective multicenter study. Int J Oral Maxillofac Implants. 2012;27:1170-1176.
- Testori T, Drago L, Wallace SS, Capelli M, Galli F, Zuffetti F, Parenti A, Deflorian M, Fumagalli L, Weinstein RL, Maiorana C, Di Stefano D, Valentini P, Giannì AB, Chiapasco M, Vinci R, Pignataro L, Mantovani M, Torretta S, Pipolo C, Felisati G, Padoan G, Castelnuovo P, Mattina R, Del Fabbro M. Prevention and treatment of postoperative infections after sinus elevation surgery: clinical consensus and recommendations. Int J Dent. 2012;2012:365809. doi: 10.1155/2012/365809. Epub 2012 Aug 9.
- Summers RB. A new concept in maxillary implant surgery: the osteotome technique. Compendium of Continuing Education in Dentistry. 1994a;15-152-160.
- Del Fabbro M, Corbella S, Weinstein T, Ceresoli V, Taschieri S. Implant survival rates after osteotome-mediated maxillary sinus augmentation: a systematic review. Clin Implant Dent Relat Res. 2012;14:s159-168.
- Mantovani M. Implicazioni otorinolaringoiatriche nell’elevazione del seno mascellare. In: La chirurgia del seno mascellare e le alternative terapeutiche. Testori T, Weinstein R, Wallace SS. Viterbo Acme, 2005
- Ludlow J, Ivanovic M. Comparative dosimetry of dental CBCT devices and 64-slice CT for oral and maxillofacial radiology. Oral Surg Oral Med Oral Pathol Oral Radiol Endod 2008;106:106-114.
- Costa CG, Tortamano IP, Rocha RG, Francischone CE, Tortamano N. Onset and duration periods of articaine and lidocaine on maxillary infiltration. Quintessence Int. 2005;36:197-201.
- Vercellotti T, De Paoli S, Nevins M. The piezoelectric bony window osteotomy and sinus membrane elevation: introduction of a new technique for simplification of the sinus augmentation procedure. Int J Periodontics Restorative Dent. 2001; 21: 561-7.
- Testori T, Rosano G, Taschieri S, Del Fabbro M. Ligation of an unusually large vessel during maxillary sinus floor augmentation. A case report. Eur J Oral Implantol 2010;3:255-8.
- Smiler D.G. The sinus lift graft: basic technique and variations Periodontics Aesthet. Dent. 1997; 9: 885-93.
- Margolin MD, Cogan AG, Taylor M, Buck D, McAllister TN, Toth C, McAllister BS. Maxillary sinus augmentation in the non-human primate: a comparative radiographic and histologic study between recombinant human osteogenic protein-1 and natural bone mineral. J Periodontol. 1998;69:911-919.
- Del Fabbro M, Testori T, Francetti L, Weinstein RL. Systematic review of survival rates for implants placed in the grafted maxillary sinus. J Periodontics Restorative Dent. 2004;24:565-577.
- Testori T, Rosano G, Taschieri S, Del Fabbro M. Ligation of an unusually large vessel during maxillary sinus floor augmentation. A case report. Eur J Oral Implantol 2010;3:255-8.
- Tarnow DP, Wallace SS, Froum SJ, Roher MD, Cho S-C. Histologic and clinical comparison of bilateral sinus floor elevations with and without barrier membrane placement in 12 patients: Part 3 of an ongoing prospective study. Int J Periodontics Restorative Dent. 2000;20:117-121.
- Tawill G, Mawla M. Sinus floor elevation using a bovine bone mineral (bio-oss) with or without the concomitant use of bilayered collagen barrier (Bio-Gide): a clinical report of immediate and delayed implant placement. Int J Oral Maxillofac Implants. 2001;16:713-721.
- Barone A, Ricci M, Grassi RF, Nannmark U, Quaranta A, Covani U. A 6-month histological analysis on maxillary sinus augmentation with and without use of collagen membranes over the osteotomy window: randomized clinical trial. Clin Oral Implants Res. 2013;24:1-6.
- García-Denche JT, Wu X, Martinez PP, Eimar H, Ikbal DJ, Hernández G, López-Cabarcos E, Fernandez-Tresguerres I, Tamimi F. Membranes over the lateral window in sinus augmentation procedures: a two-arm and split-mouth randomized clinical trials. J Clin Periodontol. 2013 Nov;40:1043-51.
- Testori T, Mandelli F, Weinstein RL, Valentini P, Wallace SS. A novel technique to prevent the loss of graft material through the antrostomy after sinus surgery: a technical note. Int J Oral Maxillofac Implants. submitted 2013.
- Wallace SS, Tarnow DP, Froum SJ, Cho SC, Zadeh HH, Stoupel J, Del Fabbro M, Testori T. Maxillary sinus elevation by lateral window approach: evolution of technology and technique. J Evid Based Dent Pract. 2012;12:161-71.
- Tarnow DP, Wallace SS, Testori T, Froum SJ, Motroni A, Prasad HS. Maxillary sinus augmentation using recombinant bone morphogenetic protein-2/acellular collagen sponge in combination with a mineralized bone replacement graft: a report of three cases. Int J Periodontics Restorative Dent. 2010;30:139-149.
- Kao DW, Kubota A, Nevins M, Fiorellini JP. The negative effect of combining rhBMP-2 and Bio-Oss on bone formation for maxillary sinus augmentation. Int J Periodontics Restorative Dent. 2012;32:61-67.
- Froum SJ, Wallace S, Cho SC, Rosenburg E, Froum S, Schoor R, Mascarenhas P, Tarnow DP, Corby P, Elian N, Fickl S, Ricci J, Hu B, Bromage T, Khouly I. A histomorphometric comparison of Bio-Oss alone versus Bio-Oss and platelet-derived growth factor for sinus augmentation: a postsurgical assessment. Int J Periodontics Restorative Dent. 2013;33:269-79.
- Del Fabbro M, Bortolin M, Taschieri S, Weinstein RL. Effect of autologous growth factors in maxillary sinus augmentation: a systematic review. Clin Implant Dent Relat Res. 2013a;15:205-216.
- Lundgren S, Andersson S, Gualini F, Sennerby L. Bone reformation with sinus membrane elevation: a new surgical technique for maxillary sinus floor augmentation Clin Implant Dent Relat Res. 2004;6:165-73.
- Cricchio G, Palma VC, Faria PE, de Olivera JA, Lundgren S, Sennerby L, Salata LA. Histological outcomes on the development of new space-making devices for maxillary sinus floor augmentation. Clin Implant Dent Relat Res. 2011;13:224-230.
- Mazor Z, Horowitz RA, Del Corso M, Prasad HS, Rohrer MD, Dohan Ehrenfest DM. Sinus floor augmentation with simultaneous implant placement using Choukroun’s platelet-rich fibrin as the sole grafting material: a radiologic and histologic study at 6 months. J Periodontol. 2009;80:2056-2064.

